Le Glaucome à Pression Normale et son Diagnostic
Comprendre le Glaucome à Pression Normale (GCAO)
Le glaucome à pression normale (GCAO) est une pathologie chronique d'évolution progressive qui reste très longtemps asymptomatique. Sa prévalence augmente avec l'âge, atteignant 1,6% chez les patients caucasiens de plus de 40 ans. Cependant, l'hypertonie oculaire n'explique pas tout, et le diagnostic est le plus souvent suspecté lors d'une visite de contrôle en raison d'antécédents familiaux de GCAO ou fortuitement lors d'une visite pour prescription de lunettes.
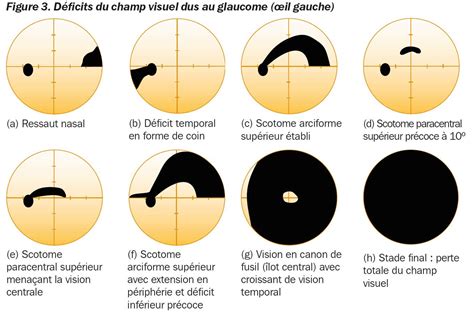
Si le patient consulte pour une altération du champ visuel ou une gêne fonctionnelle, cela signifie que le glaucome est déjà évolué. Dans les stades avancés, le champ visuel devient tubulaire, seule la vision centrale persiste.
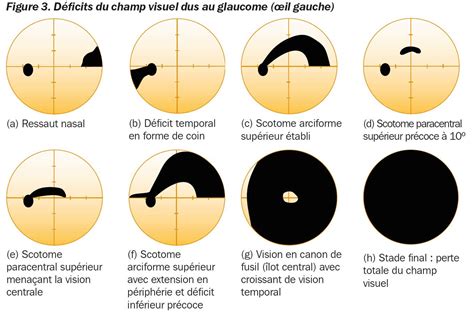
Diagnostic et Évaluation du Champ Visuel
L'exploration du champ visuel fait partie intégrante d'un examen ophtalmologique complet et est cruciale pour la détection du glaucome, des affections maculaires et des affections neurologiques telles que les accidents vasculaires cérébraux (AVC). Les déficits de champ visuel précoces, voire modérément importants, passent souvent inaperçus, en particulier s'ils n'affectent qu'un seul œil.
L'exploration du champ visuel par confrontation, bien que rapide, peut fournir des informations utiles. Ce test repose sur le principe que l'examinateur ne présente aucune anomalie du champ visuel. L'exploration débute par le champ visuel binoculaire, puis chaque œil est testé séparément, en demandant au patient de fixer l'examinateur.
Il est possible d'explorer l'hémichamp gauche du patient en plaçant son poing droit fermé dans cet hémichamp, au niveau de l'œil de l'examinateur. En levant un, deux, puis quatre doigts, on demande au patient combien il en voit. Pour explorer les quadrants supérieur et inférieur, la main est déplacée vers le haut et vers la droite, puis vers le bas et vers la droite.
Le patient doit couvrir son œil avec la paume de sa main. Le test de comptage des doigts (test statique) est effectué en premier. Ensuite, le doigt-cible est déplacé de la périphérie éloignée vers la région centrale du champ de vision (test cinétique), en demandant au patient d'indiquer quand le doigt apparaît pour la première fois dans son champ de vision. Ce test est répété dans différentes directions pour couvrir 360º pour chaque œil.
L'exploration du champ périphérique est préférablement réalisée avec une cible blanche, tandis que le champ visuel central est exploré avec une cible rouge. L'utilisation de ces cibles donne des résultats plus précis que les doigts et peut aider à détecter des déficits plus précoces du champ visuel.
Une autre méthode consiste à utiliser une grille d'Amsler. Le patient tient la grille à une distance de lecture confortable pour son œil non couvert et fixe le point central. Il doit ensuite identifier et signaler les zones où le quadrillage n'est pas visible ou apparaît déformé.
Périmétrie Statique Automatisée
Le relevé du champ visuel se fait le plus souvent à l'aide d'une périmétrie statique blanc-blanc automatisée assistée par ordinateur. Cette technique permet de cartographier les déficits du champ visuel avec précision.
Une étude comparative monocentrique prospective a évalué deux périmètres automatiques : le HFA (Humphrey Field Analyzer) et le Compass. Les patients étaient inclus après un examen complet, avec une acuité visuelle de 10/10 et une réfraction comprise entre -3 et +3 D d'équivalent sphérique. Les deux yeux étaient testés sur chaque appareil, avec un temps de repos de 30 minutes entre les tests.
Les résultats ont montré que le champ visuel de type 24-2 en stratégie SITA standard sur le HFA était comparable au 24-2 en stratégie ZEST sur le Compass en termes de Mean Deviation (MD), qui mesure le déficit moyen du champ visuel. Les valeurs de MD étaient similaires entre les deux machines : -1,6 ± 2,6 dB pour le HFA et -1,4 ± 2,8 dB pour le Compass (p=0,28).
Cependant, le Pattern Standard Deviation (PSD), qui mesure la dispersion des points du champ visuel, était significativement plus élevé pour le Compass (3,9 ± 2,4 dB) que pour le HFA (2,4 ± 1,9 dB) (p<0,0001). La durée de l'examen était également plus longue pour le Compass (351 ± 83s) par rapport au HFA (318 ± 48s) (p=0,0164).
Ces résultats suggèrent que le périmètre automatique Compass donne des résultats globalement proches de ceux du HFA, avec une comparable pour le MD, mais un PSD plus important et une durée d'examen légèrement plus longue. Ces différences, bien que statistiquement significatives, ne semblent pas majeures dans la pratique clinique courante.
L'Hypertension Intra-Oculaire (HTO) : Facteur de Risque Clé
La détection de l'hypertension intra-oculaire (HTO) et sa prise en charge représentent un élément essentiel dans la prévention ou le ralentissement de l'apparition d'un glaucome primitif à angle ouvert (GPAO), pour lequel elle constitue le principal facteur de risque contrôlable.
Définition et Prévalence
L'HTO est définie par une élévation isolée de la pression intra-oculaire (PIO) classiquement supérieure à 21 mmHg, associée à un angle iridocornéen (AIC) ouvert, mais sans altération glaucomateuse structurale de la tête du nerf optique (TNO) et des fibres nerveuses rétiniennes (FNR), et sans atteinte fonctionnelle du champ visuel (CV) aux tests cliniques standard.
La répartition de la PIO au sein de la population normale est continue, avec des valeurs s'étendant de 10 à 21 mmHg, la PIO moyenne étant de 15,5 ± 2,5 mmHg. Les PIO supérieures à 21 mmHg sont classées comme élevées. Bien que les limites supérieures de la PIO augmentent avec l'âge, il est classique de conserver la valeur de 21 mmHg comme seuil conventionnel pour définir une HTO.
La prévalence de l'HTO fluctue entre 3,5 et 12,6% selon les études, en raison des variations d'effectifs, d'ethnies et d'âges des populations étudiées. Globalement, l'HTO concerne 3 à 8% des sujets de plus de 40 ans.
L'étude observationnelle EFGH1J a rapporté une prévalence de 29% d'HTO isolée chez les patients atteints d'HTO ou de GPAO, avec une majorité de femmes (54%). L'âge moyen des patients atteints d'HTO est de 58 ans, et cette condition peut s'observer à tout âge, avec 95% des cas entre 18 et 96 ans.
La majorité des HTO (90%) se situe entre 21 et 25 mmHg. La conséquence principale d'une PIO élevée est un risque accru de GPAO.
Risque d'Évolution vers le Glaucome
Les données de la littérature rapportent un risque d'évolution vers un glaucome généralement estimé autour de 1% par an. Cependant, ce risque augmente de façon non linéaire avec le niveau de la PIO. L'étude OHTS (Ocular Hypertension Study) a montré un taux de progression vers un GPAO plus important que prévu, avec deux fois moins de glaucome chez les patients traités que dans le groupe non traité (respectivement 4,4% et 10,9%). La probabilité de développer une neuropathie glaucomateuse à 5 ans était de 4,4% pour les patients traités et de 9,5% en l'absence de traitement.
Par conséquent, un plus grand nombre d'HTO confirmées nécessiteraient d'être traitées, le risque de développer un glaucome dépendant du niveau de la PIO, car chaque millimètre de mercure additionnel augmente ce risque.
Prise en Charge et Mesure de la PIO
La découverte d'une PIO élevée doit conduire à une évaluation approfondie pour décider de la conduite à tenir. Il est essentiel de confirmer l'HTO, d'en préciser les caractéristiques, de s'assurer de son caractère isolé, et de rechercher les facteurs de risque d'évolution vers un glaucome associé.
Confirmation de l'Hypertension Intra-Oculaire
Mesure de la PIO
Le niveau de l'HTO et ses variations, propres à chaque patient, doivent être évalués. La PIO est un paramètre physiologique dynamique avec des fluctuations variables qui interviennent dans le diagnostic et la décision thérapeutique.
La constatation d'une élévation de la PIO par tonométrie à air doit être confirmée par une mesure au tonomètre par aplanation de Goldmann, qui reste la technique de référence la plus précise. Une série de trois mesures par œil est nécessaire pour obtenir une valeur moyenne fiable.
Variations Nycthémérales de la PIO
Les fluctuations à court terme de la PIO, ou variations nycthémérales sur 24 heures, varient largement entre les individus sains et glaucomateux. Bien que le rôle des fluctuations de la PIO en tant que facteur de risque de conversion de l'HTO vers le GPAO soit encore débattu, il est clairement établi que la PIO moyenne élevée constitue un facteur de risque de progression.
Les trois paramètres importants des fluctuations de la PIO corrélés avec la progression sont : le pic de la PIO, son amplitude de variation (PIO maximale - PIO minimale) et sa variation dans le temps. Les fluctuations à long terme de la PIO ne semblent pas être associées de façon significative à un risque d'apparition de GPAO chez des sujets présentant une HTO non traitée. Cependant, le niveau de la PIO moyenne initiale est un facteur de risque significatif.
Il est donc important d'évaluer avec précision le niveau de la PIO moyenne et d'apprécier ses fluctuations initiales par plusieurs mesures à différents horaires, ou par la réalisation d'une courbe diurne de la PIO. Cette courbe permet de détecter un éventuel pic de PIO au cours de la journée.
Précision de la Mesure
La qualité de la mesure de la PIO peut être influencée par divers facteurs. Le tonomètre par aplanation de Goldmann reste la technique de référence. Les tonomètres à air ont tendance à surestimer les PIO élevées et à sous-estimer les PIO basses.
Tableau 1 : Causes de surestimation de mesure de la PIO
Tableau 2 : Causes de sous-estimation de mesure de la PIO
L'épaisseur cornéenne centrale (ECC) influence également la mesure de la PIO. Une cornée épaisse peut entraîner une surestimation de la PIO avec le tonomètre de Goldmann, tandis qu'une cornée fine peut entraîner une sous-estimation. Il n'existe pas d'abaque de correction fiable pour la pratique clinique. Seuls le tonomètre de Pascal et l'Ocular Response Analyzer (ORA) permettent de s'affranchir de l'influence de l'ECC.
La mesure de l'ECC est indispensable devant toute HTO. Une ECC fine doit alerter, car elle indique une PIO réelle plus élevée que celle mesurée. Elle incite à rechercher une atteinte glaucomateuse avec une vigilance particulière.
L'analyse des propriétés biomécaniques de la cornée à l'aide de l'ORA peut fournir une valeur de PIO corrigée et compensée (PIOcc), indépendante de l'ECC. Chez les patients atteints d'HTO ou de GPAO, l'hystérésis de la cornée est diminuée, ce qui peut représenter un indicateur complémentaire potentiel.
L'HTO est-elle Isolée ?
Lorsque le diagnostic d'une HTO est posé, l'étape suivante consiste à évaluer le risque individuel qu'elle représente. Affirmer le caractère isolé de l'HTO passe par une documentation clinique initiale complète, la recherche d'un éventuel retentissement structural et fonctionnel, ainsi que par la détection de facteurs de risque d'évolution associés.
Interrogatoire
Devant tout patient présentant une HTO, la recherche des antécédents oculaires et généraux doit être systématique. L'interrogatoire précisera la présence d'antécédents familiaux d'HTO ou de GPAO, toute cause secondaire d'élévation de la PIO (traumatisme, uvéite), et l'utilisation de médicaments pouvant affecter la PIO (corticoïdes, bêtabloquants par voie générale). Les pathologies associées de type cardiovasculaire, hypertension artérielle ou hypotension artérielle, qui peuvent influencer la vascularisation de la TNO, doivent également être précisées.
Examen Clinique
Un examen ophtalmologique complet doit être réalisé pour confirmer l'absence d'une neuropathie optique glaucomateuse débutante.
Réfraction Précise
Une réfraction précise avec mesure de la meilleure acuité visuelle corrigée est essentielle pour rechercher une pathologie associée (cataracte, maculopathie, DMLA), assurer les meilleures conditions pour l'examen du champ visuel, et servir de référence pour le suivi.
Examen Biomicroscopique du Segment Antérieur
Cet examen permet d'éliminer les stigmates d'une dispersion pigmentaire, d'une pseudo-exfoliation capsulaire, ou d'une uvéite à l'origine d'une HTO secondaire, et de préciser la présence d'une phakosclérose ou d'un autre trouble des milieux pouvant perturber le relevé du champ visuel.
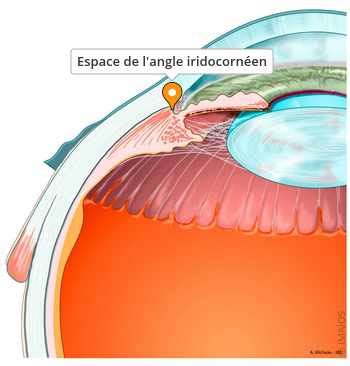
Examen Gonioscopique
L'examen gonioscopique est crucial pour évaluer l'ouverture de l'angle iridocornéen et identifier d'éventuelles anomalies structurelles.
Glaucome : causes, symptômes et traitements, Dr Roemer, Swiss Visio Network
Autres Types de Glaucome et Traitements
Le texte mentionne également d'autres variantes de glaucome :
- Glaucome pigmentaire : Variante du glaucome chronique à angle ouvert, survenant chez le sujet jeune myope.
- Glaucome exfoliatif : Variante du glaucome primitif à angle ouvert, provoqué par la dispersion d'un matériel fabriqué par le corps ciliaire, survenant chez les sujets âgés de plus de 70 ans.
- Glaucome à pression normale : Diagnostic posé devant une papille excavée ou des déficits du champ visuel, avec une PIO restant dans les normes statistiques.
- Glaucomes secondaires : Représentent 15 à 20% des glaucomes et peuvent être liés à d'autres pathologies oculaires ou systémiques.
Les traitements mentionnés incluent les collyres, notamment à base de prostaglandines et les bêta-bloquants, qui sont souvent le traitement de première intention. Des techniques chirurgicales comme la chirurgie filtrante (trabéculectomie, sclérectomie profonde) et les MIGS (Micro Invasive Glaucoma Surgery) sont également évoquées.
Le glaucome à pression normale est une pathologie qui nécessite une surveillance et une prise en charge adaptées, souvent centrées sur le contrôle de la pression intra-oculaire et la gestion des facteurs de risque vasculaires.
tags: #champ #visuel #md #psd #fpdi
