Vaccins à ARN : Composition, Fonctionnement et Applications
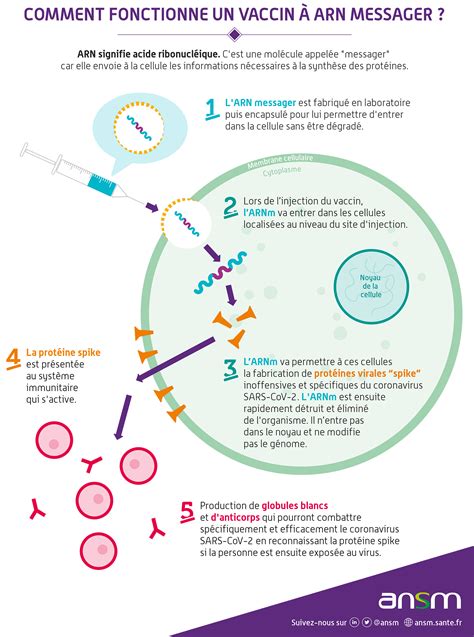
Un vaccin à ARN, également connu sous le nom de vaccin à ARN messager, est une technologie vaccinale qui active le système immunitaire adaptatif. Son mécanisme repose sur l'utilisation d'ARN messagers (ARNm) dont la séquence nucléotidique code une protéine identique ou similaire à un antigène d'agent pathogène ou tumoral. Cette protéine est ensuite produite directement dans les cellules cibles par traduction de l'ARNm contenu dans le vaccin. Le système immunitaire de l'organisme reconnaît cette protéine comme étrangère et réagit en produisant des anticorps dirigés contre l'agent pathogène ou le cancer visé.
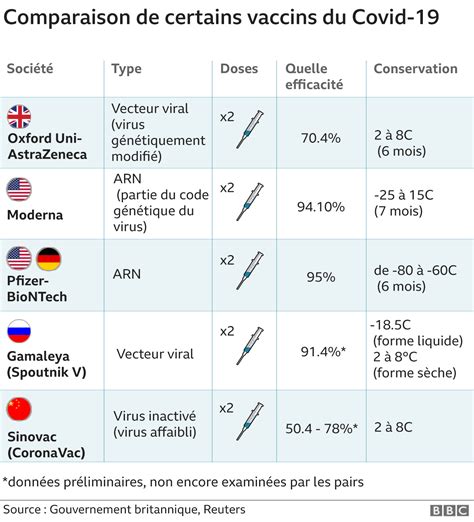
Les vaccins à ARN présentent plusieurs avantages par rapport aux vaccins à ADN, notamment en termes de fabrication, d'administration aux patients et de sécurité d'utilisation. Ils ont démontré des effets prometteurs lors d'essais cliniques sur des humains et pourraient également être bénéfiques dans le traitement de certains cancers. Plusieurs laboratoires pharmaceutiques, tels que CureVac et Moderna, développent activement ces vaccins, dont plusieurs versions ont été développées dès début 2020 pour lutter contre la COVID-19.
Fabrication et Administration des Vaccins à ARN
La fabrication d'un vaccin à ARN s'effectue généralement par transcription in vitro. L'ARN peut ensuite être introduit dans les cellules par diverses méthodes, notamment la transfection, l'électroporation (ou électroperméabilisation), la biolistique ou le transfert adoptif de cellules ex vivo. La transfection peut être facilitée par l'utilisation de nanoparticules lipidiques, de peptides de pénétration cellulaire, de protéines et de polymères. Des nanoparticules d'or d'environ 80 nm de diamètre peuvent également être employées.
Ces structures sont essentielles pour favoriser l'absorption de l'ARN par les cellules, car l'ARN est intrinsèquement instable in vivo. L'ARN absorbé par transfection pénètre dans la cellule via l'endocytose médiée par des récepteurs. La capacité d'un ARNm à être traduit en un nombre élevé de protéines est directement liée à sa stabilité. La demi-vie biologique d'un ARNm peut varier de quelques minutes à plusieurs heures, selon la protéine qu'il code.
Pour prolonger la demi-vie biologique de l'ARNm et ainsi augmenter la quantité d'antigène produite, il est possible d'utiliser des ARN auto-amplificateurs qui stimulent leur propre expression génétique. Étant sensiblement plus grands que les ARNm classiques, le mécanisme d'absorption cellulaire de ces ARN auto-amplificateurs peut différer.
Le Rôle des Cellules Dendritiques et les Voies d'Administration
Les cellules dendritiques jouent un rôle crucial dans la réponse immunitaire. En tant que phagocytes, elles présentent des antigènes sur leur membrane plasmique, interagissant ainsi avec les lymphocytes T et déclenchant une réponse immunitaire. L'intérêt pour l'administration in vivo des vaccins à ARN ne cesse de croître depuis la découverte de l'expression in vivo d'ARNm transcrits in vitro après administration directe au patient. Ces techniques offrent des avantages significatifs par rapport à l'administration ex vivo, notamment en évitant la collecte coûteuse des cellules dendritiques des patients et en mimant une infection par un agent pathogène.
Cependant, plusieurs obstacles subsistent pour rendre cette approche d'administration efficace et sûre. Il est notamment nécessaire de limiter la dégradation de l'ARN vaccinal par les ribonucléases, des enzymes qui protègent les cellules contre les acides nucléiques étrangers. L'absorption d'ARNm est connue depuis 2007, et l'utilisation d'ARN comme vaccin a été découverte dans les années 1990 sous forme d'ARNm auto-amplificateur.
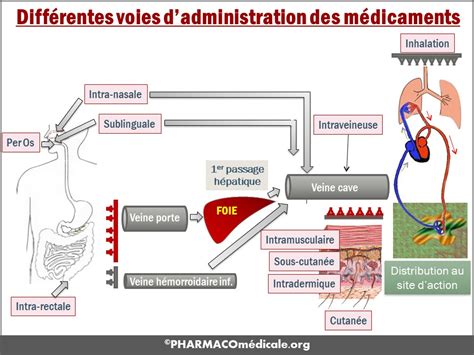
Les différentes voies d'injection (sous-cutanée, intraveineuse, intramusculaire, etc.) entraînent des niveaux d'absorption d'ARNm variés, faisant du choix du mode d'injection un facteur déterminant pour l'administration du vaccin. Il a été démontré que l'injection dans les ganglions lymphatiques conduit à la réponse la plus élevée en lymphocytes T.
Encapsulation et Stratégies d'Amélioration
L'encapsulation de l'ARNm dans des nanoparticules lipidiques présente plusieurs avantages. Premièrement, la couche lipidique protège l'ARN de la dégradation, ce qui augmente la quantité d'antigène produite. Deuxièmement, sa composition permet de cibler des cellules spécifiques de l'organisme à l'aide de ligands. La mise au point de tels vaccins reste cependant complexe, avec une absence de corrélation systématique entre l'absorption cellulaire d'ARNm observée in vitro et celle observée in vivo.
Outre les méthodes d'administration non virales, des virus à ARN ont également été modifiés pour induire un effet vaccinal. Les virus couramment utilisés à cette fin incluent les rétrovirus, les lentivirus, les alphavirus et les rhabdovirus, chacun possédant ses propres spécificités. Un avantage majeur des vaccins à ARN par rapport aux vaccins à ADN est qu'ils sont traduits dans le cytosol des cellules, évitant ainsi la nécessité de pénétrer dans les noyaux cellulaires et éliminant le risque d'incorporation de leur matériel génétique dans le génome de l'hôte.
Il est également possible d'optimiser le cadre de lecture ouvert (ORF) et les régions non traduites (UTR) des ARNm, par exemple en augmentant leur taux de GC ou en sélectionnant des régions non traduites connues pour favoriser la traduction.
Risques Potentiels et Stratégies d'Atténuation
Le principal risque associé aux vaccins à ARN est le déclenchement d'une réponse immunitaire excessive par activation du système immunitaire inné. La réponse immunitaire innée peut être activée par la liaison de l'ARN aux récepteurs de type Toll, comme la protéine TLR7, à la protéine RIG-I et à la protéine kinase R. Pour atténuer ce risque, les ARNm sont conçus avec des séquences semblables à celles produites par les cellules de mammifères. De plus, l'introduction de nucléosides modifiés dans l'ARNm, tels que la pseudouridine, la 5-méthylcytidine ou des nucléosides 2’-O-méthylés, limite la réponse immunitaire contre cet ARN étranger. Cela retarde sa dégradation et améliore son taux de traduction en antigène.
L'optimisation des codons et l'utilisation de certaines régions non traduites contribuent également à ralentir la dégradation de l'ARN. Par ailleurs, la présence de traces d'ARN bicaténaire contaminant les préparations d'ARN produites in vitro peut déclencher une interférence par ARN, conduisant à la dégradation prématurée de l'ARN vaccinal et à une réduction de sa durée d'action. Cela impose une purification en plusieurs étapes.
L'ARN extracellulaire est également connu pour favoriser la coagulation sanguine et augmenter la perméabilité de l'endothélium. L'accroissement de la perméabilité endothéliale peut entraîner un œdème et stimuler la coagulation, augmentant ainsi le risque de formation de thrombus, d'infarctus (notamment cérébral), de thrombose ou d'embolie pulmonaire.
Développements et Essais Cliniques
mRNA-1273 de Moderna
Le 16 mars 2020, le laboratoire américain Moderna a lancé un essai clinique pour son vaccin mRNA-1273, en collaboration avec le Vaccine Research Center (VRC) du National Institute of Allergy and Infectious Diseases (NIAID). Ce vaccin contient l'ARNm de la protéine S, utilisée par les coronavirus pour se lier aux cellules épithéliales. Les cellules qui absorbent cet ARNm produisent la protéine S du SARS-CoV-2, reconnue comme un corps étranger par le système immunitaire, qui stimule la formation d'anticorps protecteurs.
BNT162 de BioNTech
Le 22 avril 2020, l'Institut Paul Ehrlich (PEI) a approuvé le premier essai clinique en Allemagne pour un vaccin à ARN, le BNT162 de BioNTech. Les types d'ARNm retenus incluent l'ARNm contenant l'uridine (uRNA), l'ARNm à nucléosides modifiés (modRNA) et l'ARNm auto-amplificateur (saRNA), choisis pour leur forte immunogénicité. Les nanoparticules lipidiques (LNP) sont utilisées comme réactifs de transfection de l'ARNm, offrant stabilité après injection et capacité à pénétrer dans les cellules avec l'ARNm. Cet ARNm génère une forte réponse en anticorps et en lymphocytes T (CD8, CD4). Pfizer et BioNTech ont partagé les résultats finaux de leur vaccin contre le coronavirus, BNT162b2, le 18 novembre 2020, rapportant une efficacité supérieure à 90 % pour prévenir la COVID-19 après une seconde injection.
CVnCoV de CureVac
Le 17 juin 2020, CureVac a reçu l'accord du PEI et de l'Agence fédérale des médicaments et des produits de santé (AFMPS) de Belgique pour l'essai clinique de phase 1 de son programme de vaccination contre la COVID-19. Le vaccin potentiel induit une réponse immunitaire équilibrée et la production de lymphocytes T reconnaissant les protéines S du SARS-CoV-2. En novembre 2020, des données provisoires ont montré que le traitement était généralement bien toléré et induisait une forte réponse immunitaire. Le 14 décembre 2020, la biotech allemande a annoncé le recrutement du premier participant à l'essai clinique de phase 2b/3, qui réunira 35 000 participants, principalement en Europe et en Amérique latine. Le dosage retenu est de 12 microgrammes. Une caractéristique du vaccin CureVac est l'utilisation d'un ARNm naturel, non modifié. Par ailleurs, l'Imperial College London a lancé en juin 2020 l'essai d'une formulation d'ARN auto-amplificateur (saRNA) à nanoparticules lipidiques (LNP) nommée LNP-nCoVsaRNA. Les premiers résultats publiés le 16 juin 2021 ont indiqué une efficacité de seulement 47%, largement inférieure à celle des vaccins à ARNm de Pfizer-BioNTech et de Moderna. Des spécialistes attribuent ces résultats à une dose trop faible et à l'utilisation de nucléotides naturels entraînant une dégradation trop rapide de l'ARN.
Applications Diverses des Vaccins à ARN
Au-delà de la COVID-19, le développement des vaccins à ARN s'étend à d'autres maladies. En 2023, 23 vaccins autres que ceux contre la COVID-19 sont en phase 1, concernant 13 maladies, 6 en phase 2 pour 3 maladies et 5 en phase 3 également pour 3 maladies.
Vaccin Antigrippal
La recherche sur les vaccins antigrippaux à ARNm est soutenue dans l'Union européenne par des organismes tels que CORDIS et le projet UniVax. En 2022, une équipe de l'université de Pennsylvanie a mis au point un vaccin à ARNm immunisant contre les 20 souches connues du virus de la grippe A ou B.
Vaccin Antirabique
Ces vaccins utilisent de l'ARNm codant la glycoprotéine d'enveloppe G, principal antigène du virus de la rage. Des essais précliniques avec cet ARNm RABV encapsulé dans des nanoparticules lipidiques ont montré une meilleure réponse vaccinale chez les souris et les primates non humains.
Vaccin Personnalisé Anticancéreux
Le développement de vaccins anticancéreux à ARN est encore à ses débuts, avec des essais cliniques exploratoires. L'ARNm est transcrit à partir d'un plasmide de production en ADN, puis purifié. Le potentiel de ces traitements contre les cancers humains incurables reste à démontrer. Selon Steve Pascolo, chercheur à l'hôpital universitaire de Zurich, ces vaccins donnent d'excellents résultats lorsqu'ils sont combinés à d'autres traitements. En juin 2021, BioNTech a engagé des essais cliniques de phase II pour un vaccin à ARNm dirigé contre le mélanome. Des recherches explorent l'utilisation de nanoparticules lipidiques ciblant spécifiquement les ganglions lymphatiques pour améliorer la réponse immunitaire contre les tumeurs, tout en minimisant les réactions immunitaires indésirables telles que l'inflammation du foie.
Un vaccin contre la COVID et le cancer? La découverte résumée et analysée par un expert
Démystification des Idées Reçues
Des campagnes de désinformation affirment que les vaccins à ARN pourraient altérer l'ADN du noyau cellulaire. En réalité, l'ARNm présent dans le cytosol se dégrade très rapidement avant d'avoir le temps de pénétrer dans le noyau cellulaire. Les vaccins à ARNm nécessitent d'ailleurs une conservation à très basse température pour éviter cette dégradation. Contrairement aux rétrovirus, qui possèdent des mécanismes spécifiques pour entrer dans le noyau et utiliser la transcriptase inverse pour produire de l'ADN à partir de leur ARN, les ARNm vaccinaux ne disposent pas de ces mécanismes.
tags: #logo #corona #vectorise
